野良猫通信
国内外の食品安全関連ニュースの科学について情報発信する「野良猫 食情報研究所」。日々のニュースの中からピックアップして、解説などを加えてお届けします。
国内外の食品安全関連ニュースの科学について情報発信する「野良猫 食情報研究所」。日々のニュースの中からピックアップして、解説などを加えてお届けします。

東北大学薬学部卒、薬学博士。国立医薬品食品衛生研究所安全情報部長を退任後、野良猫食情報研究所を運営。
 畝山 智香子
畝山 智香子小林製薬の紅麹製品の問題を考える際に参考になるだろう事例が、アメリカで報告されています。今回はこの問題について2回に分けて紹介し、前編に米国の事例解説、後編はこの事例を教訓に小林製薬の紅麹製品と日本の制度について考えます。

2022年6月17日、アメリカでDaily Harvest(デイリーハーベスト)社製の「レンズ豆とリーキ(西洋ネギ)のクランブル(砕いたもの)」という製品を食べた人たちから会社に苦情が寄せられたため、製品のリコールを開始しました。本製品は、健康イメージを訴求した加工食品です。
一方、米国FDAはCFSAN有害事象報告システム(CAERS)と消費者苦情に対応して調査を開始しました。6月28日までにFDAが受け取った報告は133件でした。苦情の主な内容は消化器症状と肝機能検査の数値の異常で、2022年10月21日までにFDAが受け取ったこの製品に関する報告は393件でした。
FDAによるインシデント要約報告書は以下です。
入院患者は133人で、死亡は報告されていません。2022年の時点では病気と関連する製品は同定されていますが、その原因は同定されていません。被害者は女性が多く、平均年齢は42.7才と比較的若いです。
製品を初めてあるいは二回目に食べて24時間以内に腹痛、吐き気、嘔吐がおこり、その後発熱や疲労、数日後に黄疸や黒色尿といった症状が報告されています。6人が手術で胆のうを除去しています。
他の製品では同様の報告がないため、この製品でのみ使われた成分であるタラプロテインパウダー(Tara spinosaの種子由来粉末)が関係すると疑われました。
その後、会社はタラプロテインパウダーを使うことはなくなり、新たな患者は発生しなくなりましたが、研究者たちの原因究明は続きます。タラに含まれる特殊なアミノ酸であるバイキアインが原因ではないかという仮説が提唱(Amar G. Chittiboyina et al., Chemical Research in Toxicology 2023 36 (6), 818-821)されたりもしていますが、決定的根拠は得られていません。
タラは別途タラガムという食品添加物(E417、増粘剤)の原料でもあります。食品添加物のタラガムはタラプロテインパウダーとは製法が異なり、定められた規格があり、安全性を評価されて使われていて特に問題はありません。
そして、2024年5月にFDAがこのタラ粉末についての評価を発表しました。
結論として、タラ粉末は一般的に安全と認識される(GRAS)基準を満たさず未承認食品添加物であるため、それを使用した食品は連邦食品医薬品化粧品法(FD&C Act)のもとで安全でないとみなされる、ということです。安全でない食品は販売できません。
この判断の根拠が覚書として公表されていて、これがアメリカの新規食品の判断事例として参考になるので少し詳しく紹介したいと思います。
Scientific Memorandum: Regulatory status and review of available information pertaining to tara flour (fda.gov)
FD&C Actでは、事前承認が必要な物質や既にGRASである物質を除き、食品に使用した結果食品成分となる物質は全て「食品添加物food additive」とされます。さらに資格のある専門家が一般的に安全だと認識されている場合には食品添加物から除外されます。
タラ粉末は食品添加物として認可されていないので、GRAS要件をみたすかどうかが検討されました。
GRASかどうかを判断するためには、意図した使用条件で一般的に安全と認識されていることと安全性の根拠があることの両方が必要になります。
「一般的に安全と認識される」には
が基本となります。
1. は安全性試験のデータをそろえることになりますが、そのレベルは食品添加物として認可されるために必要なものと同等、となります。「食品添加物」なのだから当然と言えば当然ですが、食経験をもとに食品として食べられているものより高いレベルの安全性立証が必要になります。
そして、タラ粉末についてはどうかを検討します。
タラはペルーや南米で栽培されているマメ科の木で、子実体は楕円形のさやでその中に丸い種子が4~7個入っています。種子の内胚乳はタラガムに加工され、胚がタラ粉末に加工されます。タラガムの主成分はガラクトマンナン多糖類であり増粘剤として使用されていますが、胚由来タラ粉末のほうはタンパク質を多く含むという情報はあるものの、何が含まれるのか正確にはわからず、ヒトの食品として使用されたこともありません。
したがって1958年以前に米国で食品としてよく使われていたという根拠はみつかりませんでした。食経験はない、わけです。
そこで「科学的手法」による安全性の根拠を探しました。学術文献を検索した結果、タラ粉末を食品成分として安全に使える根拠となるものはみつかりませんでした。
さらにデイリーハーベスト社の製品回収後の各種研究など、まだ論文として発表されていない追加の情報も検討しています。そして回収対象製品を摂取して体調不良を訴えた人たちの記録ももちろん検討しました。
結果としてタラ粉末には深刻な安全上の懸念があり、食品成分として安全に使えることを支持するデータはないと判断されました。したがってタラ粉末はGRASではなく、未承認食品添加物であるため、それを使用した食品は安全でないとみなされる、わけです。
なおこの段階でもタラ粉末が報告された多数の健康被害の原因であるとは結論できていません。因果関係を立証するのは簡単ではないのです。
またカナダでは、2023年9月にタラプロテインパウダー(タラ粉末)を含む食品を販売したり購入したりしないように企業向けの通知を出しているとの追加情報もあります。
新規食品に分類される可能性の高い物質であり、新規食品は事前に安全性評価を経なければ販売できないからです。アメリカとカナダは、法律上の文言は異なりますが実質的には同等の安全性の判断をしていると言えます。
このデイリーハーベストのタラ粉末の事件は小林製薬の紅麹製品の事件に似ているところがあり、米国での対応を日本だったらどうなるだろうと考えると興味深いと思います。(後編に続く)

東北大学薬学部卒、薬学博士。国立医薬品食品衛生研究所安全情報部長を退任後、野良猫食情報研究所を運営。
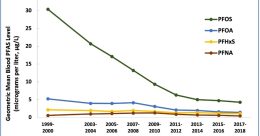 PFASの血中濃度 元情報を確認して正確な報道を
PFASの血中濃度 元情報を確認して正確な報道を  米国の食品の被害事例―小林製薬の紅麹製品と比べると(後)
米国の食品の被害事例―小林製薬の紅麹製品と比べると(後) 国内外の食品安全関連ニュースの科学について情報発信する「野良猫 食情報研究所」。日々のニュースの中からピックアップして、解説などを加えてお届けします。
