投稿コーナー
連載陣とは別に、多くの方々からのご寄稿を受け付けます。info@foocom.netへご連絡ください。事務局で検討のうえ、掲載させていただきます。お断りする場合もありますので、ご了承ください
連載陣とは別に、多くの方々からのご寄稿を受け付けます。info@foocom.netへご連絡ください。事務局で検討のうえ、掲載させていただきます。お断りする場合もありますので、ご了承ください
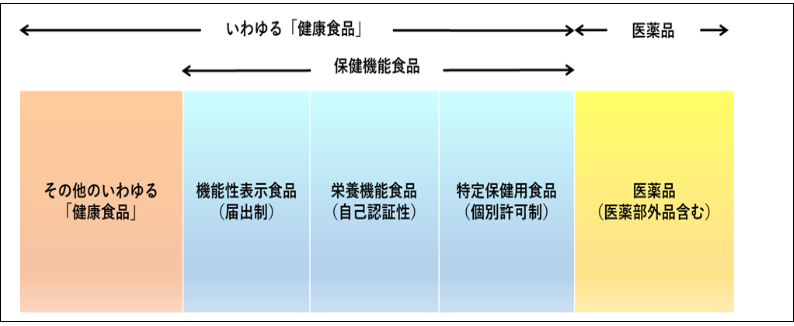
健康への何らかの効果を期待して経口摂取する医薬品以外の食品が「いわゆる『健康食品』」であり(1)、通常の食材や菓子、飲料のほか、錠剤、カプセル、粉末など、形態は様々である。それらのうち、「国が定めた安全性や有効性に関する基準等を満たした」のが保健機能食品で機能性を表示できる。現時点において特定保健用食品(1991年~)、栄養機能食品(2001年~)、機能性表示食品(2015年~)の3種類がある。保健機能食品以外の「いわゆる『健康食品』」は「その他のいわゆる『健康食品』」である。(下図)
しかしながら「国が定めた安全性や有効性に関する基準を満たした」はずの機能表示食品に重大な健康被害が起きたらしい。商品を製造・販売した小林製薬株式会社が2024年3月22日(金)の18時から約1時間50分にわたり「紅麹関連製品の使用中止のお願いと自主回収のおしらせに関する緊急記者会見」と題する会見を開いたのである。記者会見には同社社長のほか、製造本部長(執行役員)、信頼性保証本部長(執行役員)、ヘルスケア事業部食品カテゴリー長の計4人が出席していた。会見の冒頭、社長は「弊社が販売している『紅麹コレステヘルプ』を摂取した人に腎疾患などが発生していることを受け、成分分析を行った結果、一部の紅麹原料に本来想定していない成分が含まれている可能性があることが判明。健康被害の拡大を防ぐために紅麹関連製品を自主回収する。早期に製品使用を中止してもらうために会見を開いた」との旨を述べた。
続く約15分間は信頼性保証本部長が紅麹製品の製造方法や被害事象などについて説明し、その後に質疑応答が行われた。記者会見から私が理解したことはおよそ以下のことである。
健康被害事例は本人または医師からの申し出により13名(通院治療7名、入院治療6名(5名は退院、1名は今も入院中))で、2024年1月11日から3月15日までのおよそ2ヶ月間に及ぶ。居住地域、年齢、性別、病状の程度等は個人情報のため開示できないとのことで詳細は不明である。
患者を治療した複数の医師から紅麹菌が生成するカビ毒・シトリニンが原因物質ではないかとの指摘を受けたが、元々シトリニンを生成しない紅麹の菌株を使っており、検査結果も不検出だった。また、この製品の機能性関与成分は「米紅麹ポリケチド」であるがポリケチドは多量摂取により横紋筋融解症を起こすことがあるとの情報がある。それによる腎臓への悪影響も考えられるが医師からその所見はないと否定された。さらにアレルギーの可能性についてはDSLT(drug -induced lymphocyte stimulation)に陽性を示した人も複数いて、薬剤アレルギーの可能性があるとのことだった。
いくつかの可能性を検討していく中で、一部の製品ロットと紅麹原料のロットから未知の波形のピークを90ロット中、18ロットから検出したとの報告を3月17日17時に開発部門から受け、直ちに執行役員会議メンバーによる緊急会議を行い、3月22日に臨時取締役会、そしてニュースリリースし、この記者会見に臨んだ。「未知のピーク物質」はまだ特定できておらず、複数の大学の研究室と共同で確認作業を進めている。
質疑応答において、機能性表示食品であることを問題視する発言が出てこないことにいらだっていると会見開始から約1時間20分たった頃、「NHKの山本」と名乗る人物が「この商品は機能性表示食品。安全面などに関する調査はどうだったのか」と質問した。回答は「当時としてやるべき事はやった上で届け出て受理された」だった。連鎖的に保健機能食品という枠組みの中の機能性表示食品であることに関連する質問を期待したが無駄だった。
この件を私が知ったのは3月22日19時のNHKのラジオニュースだった。車の運転中で「小林製薬が健康食品の自主回収を・・・」との報道に感じたのは、「またか」だった。ラジオニュースでは一言も「機能性表示食品」とは言わなかったからである。21時からの「ニュースウオッチ9」も同様で「機能性表示食品」との発言はなかった。だから、まさか保健機能食品である機能性表示食品で健康被害とは思ってもみなかったのである。傍らでニュースを見ていた家人から、「これって、ほら、ただの健康食品じゃなくって、なんとかなんじゃないの?」と問われて、「トクホとか機能性表示食品とか?いやー、一言もそんなこと言ってないからそれはないでしょ。」と返答。しかし、もしやと思って検索すると、なんと機能性表示食品ではないか。目を疑った。
保健機能食品についてその存在意義等について批判し続けている私であるが、油断していたようである。「国の定めた・・・・」に私自身が惑わされ、「その他のいわゆる『健康食品』」のような健康被害は起こり得ないと思い込んでしまっていたのかもしれない。それを反省するとともにNHKのニュース記事執筆者はこの事例の重大性がわかっていないと感じた。
機能性表示食品は「疾患を持たない、妊産授乳婦・妊娠計画者でもない成人を利用対象者とし、事業者の責任において、科学的根拠に基づいた機能性を表示した食品で、販売前に安全性と機能性の根拠に関する情報などを消費者庁長官へ届け出たもの」である。時の総理大臣のかけ声のもと、簡易版特定保健用食品として、経済活性化策のひとつとして2015年度から始まった。「特定保健用食品は許可を得るための手続が大変なので、もっと簡単に機能性を表示できるようにすべきである」との規制改革会議の答申(2013/6/5)に基づき、2年をかけずに大急ぎで作られた、別称「機能性届出食品」「ミニトクホ」である。
届出が受理された機能性表示食品の情報は消費者庁のウェブサイトに設けられた「機能性表示食品の検索」(2)システムを利用すると得られる。1週間から10日に一度ほどで更新される。届出商品に与えられた届出番号や商品名を入力するとその商品に関する機能性や安全性に関する情報を閲覧できる。
健康被害をもたらした当該商品の「科学的根拠などに関する基本情報」(3)を閲覧すると最初に「1.安全性に関する基本情報」が出てくる。「1.食経験の評価」として「当該製品と製品名のみ異なる同一処方の製品を2018 年から20万食以上販売しているが、本製品が原因と示唆される重篤な健康被害は報告されていない。(後略)」とあり、「2.安全性試験の評価」には「当該製品の原材料の紅麹を用いて、マウス急性経口毒性試験、ラット90日間反復投与毒性試験、復帰突然変異試験、染色体異常誘発試験、薬物相互作用試験、ヒト過剰摂取試験、ヒト長期服用試験などを実施し、すべての検査項目で安全性に問題は認められなかった。」と続き、「3.まとめ」には「以上のことから、当該製品を適切に摂取するには安全であると考えられる。」と結論している。今となってはむなしい記述である。
この記者会見は金曜日の午後6時からの開催だった。私は群馬県前橋市在住で、いわゆる全国紙である新聞を購読しているが、届いた3月23日の朝刊紙面にこの件の記事はなかった。印刷配布の関係で記事掲載が間に合わなかったと思われるが、翌24日の朝刊にも記事はなかった。ところが今朝(25日)の紙面には小林製薬の記者会見の記事はないまま、同社の紅麹原料を使った日本酒を回収するとの記事が掲載されていた。ここにも事の重大性の認識不足を感じた。
食品の「機能性成分」とは食品中にわずかに含まれる栄養素ではない、しかし、生体機能の調節や健康維持に有効と考えられる物質のことである。それらを摂取するとその「機能性」が発揮され、健康が得られるかのような錯覚が世の中に蔓延している。これを私は「機能性幻想」と呼んでいる。ある機能性成分を、機能性を発揮するという量で摂取しても万人にその「機能」(効果)が発現するわけではない。それどころか今回の自主回収対象商品は利用者の一部に健康被害をもたらしたのかもしれないのである。
「機能性幻想」は一歩間違えば健康被害をもたらす可能性があり、過去に何度かこのような事例は繰り返されてきた。今後、この件に関して当該企業だけでなく、消費者庁をはじめとする行政機関がどのよう対応するのか、また、機能性表示食品制度そのものの廃止を視野に入れた検討はされないのか、注視していきたい。
(1)https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou_iryou/shokuhin/hokenkinou/index.html
(2) https://www.fld.caa.go.jp/caaks/cssc01/
(3) https://www.fld.caa.go.jp/caaks/cssc02/?recordSeq=42403220781001
 豊年満作を呼ぶ昆虫たち
豊年満作を呼ぶ昆虫たち  紅麹サプリ問題を2016年の著書で警告(畝山智香子さん)
紅麹サプリ問題を2016年の著書で警告(畝山智香子さん) 連載陣とは別に、多くの方々からのご寄稿を受け付けます。info@foocom.netへご連絡ください。事務局で検討のうえ、掲載させていただきます。お断りする場合もありますので、ご了承ください
